Chlorotrifluorométhane
| Chlorotrifluorométhane | |||
 | |||
 | |||
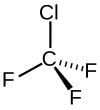
| représentation du chlorotrifluorométhane | |||
| Identification | |||
|---|---|---|---|
| Nom UICPA | chlorotrifluorométhane | ||
| Synonymes | chlorure de trifluorométhane | ||
| No CAS | 75-72-9 | ||
| No ECHA | 100.000.814 | ||
| No CE | 200-894-4 | ||
| PubChem | 6392 | ||
| SMILES | C(F)(F)(F)Cl PubChem, vue 3D | ||
| InChI | InChI : vue 3D InChI=1S/CClF3/c2-1(3,4)5 | ||
| Apparence | gaz incolore, inodore sauf en très grande concentration (odeur douce éthérée, proche de celle du tétrachlorométhane) | ||
| Propriétés chimiques | |||
| Formule | CClF3 [Isomères] | ||
| Masse molaire[2] | 104,459 ± 0,003 g/mol C 11,5 %, Cl 33,94 %, F 54,56 %, | ||
| Moment dipolaire | 0,50 ± 0,01 D [1] | ||
| Propriétés physiques | |||
| T° fusion | −189 °C[3] | ||
| T° ébullition | −81,4 °C[3] | ||
| Solubilité | 0,09 g·l-1 à 20 °C[4] | ||
| Masse volumique | 4,404 kg·m-3 (gaz, 1 bar, 15 °C)[3] | ||
| T° d'auto-inflammation | Ininflammable | ||
| Pression de vapeur saturante | 19,7 bar à 0 °C 25,2 bar à 10 °C 31,759 bar à 20 °C[3] | ||
| Point critique | 28,78 °C 38,6 bar 0,581 kg·l-1[3] | ||
| Propriétés électroniques | |||
| 1re énergie d'ionisation | 12,6 ± 0,2 eV (gaz)[5] | ||
| Précautions | |||
| SIMDUT[6] | |||
 A, A : Gaz comprimé température critique = 28,8 °C Divulgation à 1,0% selon les critères de classification | |||
| Directive 67/548/EEC | |||
 N Symboles : N : Dangereux pour l’environnement Phrases R : R59 : Dangereux pour la couche d’ozone. Phrases S : S9 : Conserver le récipient dans un endroit bien ventilé. S23 : Ne pas respirer les gaz/fumées/vapeurs/aérosols [terme(s) approprié(s) à indiquer par le fabricant]. S59 : Consulter le fabricant/fournisseur pour des informations relatives à la récupération/au recyclage. Phrases R : 59, | |||
| Transport | |||
Code Kemler : 20 : gaz asphyxiant ou qui ne présente pas de risque subsidiaire Numéro ONU : 1022 : CHLOROTRIFLUOROMÉTHANE ; ou GAZ RÉFRIGÉRANT R 13 Classe : 2.2 Étiquette :  2.2 : Gaz ininflammables, non toxiques (correspond aux groupes désignés par un A ou un O majuscule); | |||
| Unités du SI et CNTP, sauf indication contraire. | |||
modifier  | |||
Le chlorotrifluorométhane CClF3, également appelé fréon 13, CFC-13, ou R-13, est un halogénoalcane de la famille des chlorofluorocarbures (CFC). C'est un gaz ininflammable, non-corrosif, incolore, inodore (sauf en très grande concentration où son odeur est douce et éthérée, proche de celle du tétrachlorométhane).
Il est utilisé comme réfrigérant sous le nom de R-13, mais du fait de la dégradation de l'ozone qu'il engendre, son usage est de plus en plus réduit. Le Protocole de Montréal a décidé l'arrêt total de sa production en 2010[7].
Propriétés
Notes et références
- ↑ (en) David R. Lide, Handbook of chemistry and physics, Boca Raton, CRC, , 89e éd., 2736 p. (ISBN 978-1-4200-6679-1 et 1-4200-6679-X), p. 9-50
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ a b c d et e Entrée du numéro CAS « 75-72-9 » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 30/05/09 (JavaScript nécessaire)
- ↑ fiche CSST
- ↑ (en) David R. Lide, Handbook of chemistry and physics, Boca Raton, CRC, , 89e éd., 2736 p. (ISBN 978-1-4200-6679-1), p. 10-205
- ↑ « Chlorotrifluorométhane » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- ↑ Annexe B, Protocole de Montréal relatif à des substances qui appauvrissent la couche d'ozone, 1522 RTNU 3, 26 ILM 1541 (entrée en vigueur: ) (en ligne: https://www.actu-environnement.com/media/pdf/texte_protocole_de_montreal.pdf [archive]), page consultée le 4 mai 2019.
v · m Halogénométhanes | |
|---|---|
| Monosubstituté |
|
| Disubstituté |
|
| Trisubstituté |
|
| Tétrasubstituté |
|
v · m | |
|---|---|
| Fluorures F(-I) |
|
| Interhalogènes |
|
| Tétrafluoroborates |
|
| Composés AlF6, AsF6, SbF6... |
|
| Composés NbF7, TaF7 |
|
| Perfluorocarbures |
|
| Hydrocarbures halogénés |
|
| Bifluorures |
|
| Oxohalogénures |
|
v · m | |
|---|---|
| Chlorures Cl(-I) |
|
| Interhalogènes | |
| Composés BCl4, AuCl4 |
|
| Composés AlCl6, PCl6... |
|
| Composés NbCl7, TaCl7 |
|
| Perchlorocarbures |
|
| Hydrocarbures halogénés |
|
| Oxohalogénures | |
 Portail de la chimie
Portail de la chimie








