Benzonitrila
| Benzonitrila Alerta sobre risco à saúde | |
|---|---|
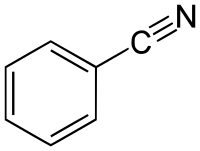 | |
| Nome IUPAC | Benzonitrile |
| Outros nomes | cianobenzeno Cianeto de fenila fenilcianeto ácido bezóico nitrila |
| Identificadores | |
| Número CAS | 100-47-0 |
| PubChem | 7505 |
| SMILES |
|
| InChI | 1/C7H5N/c8-6- 7-4-2-1-3-5-7/h1-5H |
| Propriedades | |
| Fórmula molecular | C7H5N |
| Massa molar | 103.04 g/mol |
| Densidade | 1.0 g/ml |
| Ponto de fusão | −13 °C |
| Ponto de ebulição | 188–91 °C |
| Solubilidade em água | <0.5 g/100 ml (22 °C) |
| Índice de refracção (nD) | 1.5280 |
| Riscos associados | |
| Classificação UE | Nocivo (Xn) |
| Índice UE | 608-012-00-3 |
| NFPA 704 |  2 3 0 |
| Frases R | R21/22 |
| Frases S | S2, S23 |
| Ponto de fulgor | 75 °C |
| Temperatura de auto-ignição | 550 °C |
| Limites de explosividade | 1.4–7.2% |
| Número RTECS | DI2450000 |
| Compostos relacionados | |
| Compostos relacionados | Benzilamina |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Benzonitrila é o composto químico com a fórmula C6H5CN, abreviadamente PhCN (do inglês phenil). Este composto orgânico aromático é incolor, com um odor de amêndoas doces. É preparado pela desidratação de benzamida, ou pela reação de cianeto de sódio com bromobenzeno.
Aplicações
Benzonitrila é um solvente útil e um precursor versátil de muitos derivados. Ele reage com aminas resultando N-benzamidas substituídas após hidrólise.[1] É um precursor para Ph2C=NH (difenilquetimina ou difenilmetilenimina, p.e. 151 °C, 8 mm Hg) via reação com brometo de fenilmagnésio seguido por metanólise.[2]
Benzonitrila pode formar compostos de coordenação com os últimos metais de transição que são tanto solúveis em solventes orgânicos e convenientemente lábeis, e.g. PdCl2(PhCN)2. Os ligantes benzonitrila são prontamente deslocados por ligantes mais fortes, fazendo complexos de benzonitrila intermediários sintéticos úteis.[3]
Referências
- ↑ Cooper, F.C.; Partridge, M. W. (1963). «N-Phenylbenzamidine». Org. Synth. !CS1 manut: Nomes múltiplos: lista de autores (link); Coll. Vol., 4
- ↑ Pickard, P. L.; Tolbert, T. L. (1973). «Diphenyl Ketimine». Org. Synth. !CS1 manut: Nomes múltiplos: lista de autores (link); Coll. Vol., 5
- ↑ Gordon K. Anderson, Minren Lin (1990). «Bis(Benzonitrile)Dichloro Complexes of Palladium and Platinum». Inorganic Syntheses. 28: 60–63. doi:10.1002/9780470132593.ch13
Ligações externas
- BENZONITRILA - Ficha de Informação de Produto Químico - www.cetesb.sp.gov.br











 Benzonitrila
Benzonitrila