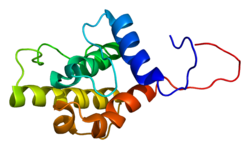
| L-пластин |
|---|
 |
| Наявні структури |
|---|
| PDB | Пошук ортологів: PDBe RCSB |
|---|
| |
| Ідентифікатори |
|---|
| Символи | LCP1, CP64, HEL-S-37, L-PLASTIN, LC64P, LPL, PLS2, lymphocyte cytosolic protein 1 |
|---|
| Зовнішні ІД | OMIM: 153430 MGI: 104808 HomoloGene: 80174 GeneCards: LCP1 |
|---|
| |
| Пов'язані генетичні захворювання |
|---|
| fatty liver disease[1] |
| Онтологія гена |
|---|
| Молекулярна функція | • calcium ion binding
• зв'язування з іоном металу
• actin filament binding
• identical protein binding
• GTPase binding
• actin binding
• integrin binding
|
|---|
| Клітинна компонента | • цитоплазма
• гіалоплазма
• cell projection
• мембрана
• focal adhesion
• Філоподія
• ruffle
• клітинна мембрана
• stress fiber
• ruffle membrane
• мікрофіламент
• actin cytoskeleton
• actin filament bundle
• podosome
• phagocytic cup
• екзосома
• цитоскелет
• міжклітинний простір
• міжклітинні контакти
• perinuclear region of cytoplasm
|
|---|
| Біологічний процес | • extracellular matrix disassembly
• positive regulation of podosome assembly
• actin filament bundle assembly
• regulation of intracellular protein transport
• animal organ regeneration
• protein kinase A signaling
• cell migration
• wound healing, spreading of cells
• T cell activation involved in immune response
• actin filament network formation
• actin crosslink formation
• interleukin-12-mediated signaling pathway
|
|---|
| Джерела:Amigo / QuickGO | |
| Шаблон експресії |
|---|
 |
| Більше даних |
| Ортологи |
|---|
| Види | Людина | Миша |
|---|
| Entrez | | |
|---|
| Ensembl | | |
|---|
| UniProt | | |
|---|
| RefSeq (мРНК) | | |
|---|
| RefSeq (білок) | | |
|---|
| Локус (UCSC) | Хр. 13: 46.13 – 46.21 Mb | Хр. 14: 75.37 – 75.47 Mb |
|---|
| PubMed search | [2] | [3] |
|---|
| Вікідані |
| Див./Ред. для людей | Див./Ред. для мишей |
|
L-пластин (англ. Lymphocyte cytosolic protein 1) – білок, який кодується геном LCP1, розташованим у людей на короткому плечі 13-ї хромосоми. [4] Довжина поліпептидного ланцюга білка становить 627 амінокислот, а молекулярна маса — 70 288[5].
Послідовність амінокислот
| 10 | | 20 | | 30 | | 40 | | 50 |
|---|
| MARGSVSDEE | | MMELREAFAK | | VDTDGNGYIS | | FNELNDLFKA | | ACLPLPGYRV |
| REITENLMAT | | GDLDQDGRIS | | FDEFIKIFHG | | LKSTDVAKTF | | RKAINKKEGI |
| CAIGGTSEQS | | SVGTQHSYSE | | EEKYAFVNWI | | NKALENDPDC | | RHVIPMNPNT |
| NDLFNAVGDG | | IVLCKMINLS | | VPDTIDERTI | | NKKKLTPFTI | | QENLNLALNS |
| ASAIGCHVVN | | IGAEDLKEGK | | PYLVLGLLWQ | | VIKIGLFADI | | ELSRNEALIA |
| LLREGESLED | | LMKLSPEELL | | LRWANYHLEN | | AGCNKIGNFS | | TDIKDSKAYY |
| HLLEQVAPKG | | DEEGVPAVVI | | DMSGLREKDD | | IQRAECMLQQ | | AERLGCRQFV |
| TATDVVRGNP | | KLNLAFIANL | | FNRYPALHKP | | ENQDIDWGAL | | EGETREERTF |
| RNWMNSLGVN | | PRVNHLYSDL | | SDALVIFQLY | | EKIKVPVDWN | | RVNKPPYPKL |
| GGNMKKLENC | | NYAVELGKNQ | | AKFSLVGIGG | | QDLNEGNRTL | | TLALIWQLMR |
| RYTLNILEEI | | GGGQKVNDDI | | IVNWVNETLR | | EAKKSSSISS | | FKDPKISTSL |
| PVLDLIDAIQ | | PGSINYDLLK | | TENLNDDEKL | | NNAKYAISMA | | RKIGARVYAL |
| PEDLVEVNPK | | MVMTVFACLM | | GKGMKRV |
Білок має сайт для зв'язування з молекулою актину, іонами металів, іоном кальцію. Локалізований у клітинній мембрані, цитоплазмі, цитоскелеті, мембрані, клітинних контактах, клітинних відростках.
Література
- The status, quality, and expansion of the NIH full-length cDNA project: the Mammalian Gene Collection (MGC). Genome Res. 14: 2121—2127. 2004. PMID 15489334 DOI:10.1101/gr.2596504
- Lin C.-S., Aebersold R.H., Kent S.B., Varma M., Leavitt J. (1988). Molecular cloning and characterization of plastin, a human leukocyte protein expressed in transformed human fibroblasts. Mol. Cell. Biol. 8: 4659—4668. PMID 3211125 DOI:10.1128/MCB.8.11.4659
- Lin C.-S., Aebersold R.H., Leavitt J. (1990). Correction of the N-terminal sequences of the human plastin isoforms by using anchored polymerase chain reaction: identification of a potential calcium-binding domain. Mol. Cell. Biol. 10: 1818—1821. PMID 2378651 DOI:10.1128/MCB.10.4.1818
- Matsushima K., Shiroo M., Kung H.F., Copeland T.D. (1988). Purification and characterization of a cytosolic 65-kilodalton phosphoprotein in human leukocytes whose phosphorylation is augmented by stimulation with interleukin 1. Biochemistry. 27: 3765—3770. PMID 3261603 DOI:10.1021/bi00410a037
- Carrascal M., Ovelleiro D., Casas V., Gay M., Abian J. (2008). Phosphorylation analysis of primary human T lymphocytes using sequential IMAC and titanium oxide enrichment. J. Proteome Res. 7: 5167—5176. PMID 19367720 DOI:10.1021/pr800500r
- Lin C.-S., Park T., Chen Z.P., Leavitt J. (1993). Human plastin genes. Comparative gene structure, chromosome location, and differential expression in normal and neoplastic cells. J. Biol. Chem. 268: 2781—2792. PMID 8428952
Примітки
- ↑ Захворювання, генетично пов'язані з L-пластин переглянути/редагувати посилання на ВікіДаних.
- ↑ Human PubMed Reference:.
- ↑ Mouse PubMed Reference:.
- ↑ HUGO Gene Nomenclature Commitee, HGNC:6528 (англ.) . Архів оригіналу за 14 жовтня 2017. Процитовано 30 січня 2017.
- ↑ UniProt, P13796 (англ.) . Архів оригіналу за 24 січня 2017. Процитовано 30 січня 2017.
Див. також
 | Це незавершена стаття про білки.
Ви можете допомогти проєкту, виправивши або дописавши її. |
 Портал «Біологія» Портал «Біологія»  Портал «Хімія» Портал «Хімія»
|
| На цю статтю не посилаються інші статті Вікіпедії. Будь ласка розставте посилання відповідно до прийнятих рекомендацій. |














 L-пластин
L-пластин